Hasta el siglo XIX se explicaba el efecto del ambiente en la variación de la temperatura de un cuerpo por medio de un fluido invisible llamado calórico. Este se producía cuando algo se quemaba y, además, que podía pasar de un cuerpo a otro. La teoría del calórico afirmaba que una sustancia con mayor temperatura que otra, necesariamente, poseía mayor cantidad de calórico.
Benjamin Thompson y James Prescott Joule establecieron que el trabajo podía convertirse en calor o en un incremento de la energía térmica determinando que, simplemente, era otra forma de la energía.
El Calor
El calor está definido como la forma de energía que se transfiere entre diferentes cuerpos o diferentes zonas de un mismo cuerpo que se encuentran a distintas temperaturas, sin embargo en termodinámica generalmente el término calor significa simplemente transferencia de energía. Este flujo de energía siempre ocurre desde el cuerpo de mayor temperatura hacia el cuerpo de menor temperatura, ocurriendo la transferencia hasta que ambos cuerpos se encuentren en equilibrio térmico (ejemplo: una bebida fría dejada en una habitación se entibia).
La energía puede ser transferida por diferentes mecanismos de transferencia, estos son la radiación, la conducción y la convección, aunque en la mayoría de los procesos reales todos se encuentran presentes en mayor o menor grado. Cabe resaltar que los cuerpos no tienen calor, sino energía térmica. La energía existe en varias formas. En este caso nos enfocamos en el calor, que es el proceso mediante el cual la energía se puede transferir de un sistema a otro como resultado de la diferencia de temperatura.
Calor en el Ser Humano
Generalmente en la mayoría de los países, se habla ya de calor cuando la temperatura supera los 26 ºC en cualquier hora del día, aunque varía mucho según la estación del año en que se encuentre una persona. Por ejemplo, 20º C en verano es considerado una temperatura fresca, mientras que en invierno, esta temperatura es considerada templada o cálida.
El fenómeno "ola de calor" se da cuando las temperaturas diurnas superan los 32 ºC y las nocturnas (o al amanecer) no bajan de los 23 ºC por 3 días y es común en casi todo tipo de climas en época veraniega, a excepción de los países cerca de los polos, con clima templado y polar, cuando es muy infrecuente o casi nulo, y se hace más frecuente cuando los países están más cerca de los trópicos (países con climas tropical y subtropical). Esta denominación de ola de calor no quiere decir necesariamente calor excesivo ni temperaturas inusuales para la estación; pretende alertar sobre consecuencias perjudiciales en personas o colectivos vulnerables.
El ser humano siente más calor cuando hay más humedad en el ambiente. Por ejemplo, una temperatura de 30 ºC, pero con humedad ambiental del 10%, se sentirá como si el ambiente fuese de solo 28º C. Pero con humedad ambiental del 90%, se sentirá como si el ambiente fuese de 40 ºC.
Unidades de Medida
La unidad de medida del calor en el Sistema Internacional de Unidades es la misma que la de la energía y el trabajo: el Joule.
Otra unidad ampliamente utilizada para medir la cantidad de energía térmica intercambiada es la caloría (cal), que es la cantidad de energía que hay que suministrar a un gramo de agua para elevar su temperatura 1 °C. Diferentes condiciones iniciales dan lugar a diferentes valores para la caloría. La caloría también es conocida como caloría pequeña, en comparación con la kilocaloría (kcal), que se conoce como caloría grande y es utilizada en nutrición.
1 kcal = 1000 cal
Joule, tras múltiples experimentaciones en las que el movimiento de unas palas, impulsadas por un juego de pesas, se movían en el interior de un recipiente con agua, estableció el equivalente mecánico del calor, determinando el incremento de temperatura que se producía en el fluido como consecuencia de los rozamientos producidos por la agitación de las palas:
1 cal = 4,184 J1
El BTU, (o unidad térmica británica) es una medida para el calor muy usada en Estados Unidos y en muchos otros países de América. Se define como la cantidad de calor que se debe agregar a una libra de agua para aumentar su temperatura en un grado Fahrenheit, y equivale a 252 calorías.
Calor Especifico
El calor específico es la energía necesaria para elevar 1 °C la temperatura de un gramo de materia. El concepto de capacidad calorífica es análogo al anterior pero para una masa de un mol de sustancia (en este caso es necesario conocer la estructura química de la misma).
El calor específico es un parámetro que depende del material y relaciona el calor que se proporciona a una masa determinada de una sustancia con el incremento de temperatura:
donde:
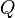 es el calor aportado al sistema.
es el calor aportado al sistema.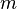 es la masa del sistema.
es la masa del sistema. es el calor específico del sistema.
es el calor específico del sistema. es el incremento de temperatura que experimenta el sistema.
es el incremento de temperatura que experimenta el sistema.
Las unidades más habituales de calor específico son J / (kg · K) y cal / (g · °C).
El calor específico de un material depende de su temperatura; no obstante, en muchos procesos termodinámicos su variación es tan pequeña que puede considerarse que el calor específico es constante. Asimismo, también se diferencia del proceso que se lleve a cabo, distinguiéndose especialmente el "calor específico a presión constante" (en un proceso isobárico) y "calor específico a volumen constante (en un proceso isocórico).
De esta forma, y recordando la definición de caloría, se tiene que el calor específico del agua es aproximadamente:







